2025年7月17日,我校张泽民教授团队及合作者在Cancer Cell杂志发表题为“Integrated Single-Cell and Spatial Transcriptomics Uncover Distinct Cellular Subtypes Involved in Neural Invasion in Pancreatic Cancer”的研究长文,揭示了胰腺导管腺癌发生神经束侵袭转移的细胞及分子机制。

被称为“癌王”的胰腺导管腺癌(Pancreatic Ductal Adenocarcinoma, PDAC)高发神经侵犯(Neural Invasion, NI),严重影响病人预后及生存质量。外科医生在临床实践中发现,局部神经清扫手术能减少病人术后复发,但其原因及机制尚未清晰。
为了描绘胰腺癌的“神经暗网”地图,研究者对25例PDAC患者的62例样本进行了单细胞/单细胞核测序及空间转录组测序,结合mIHC、病理形态学分析及体外实验,系统对比不发生神经侵犯与发生神经侵犯的胰腺癌组织,刻画了人胰腺癌组织中神经束的内外微环境,解析了肿瘤相关神经束的具体细胞组分及其与癌细胞、免疫细胞和基质细胞的相互作用,揭示了癌细胞发生神经束侵袭转移(Neural Invasion, NI)的细胞及分子机制。研究 发现低神经侵犯与高神经侵犯的组织有着显著的组成差异。低NI的肿瘤组织中,有更多的终末分化效应记忆性CD8 T细胞(terminally differentiated effector memory T cells,Temra)、B细胞、浆细胞,提示可能有更多三级淋巴结构(Tertiary Lymphoid Tissues, TLSs)的形成。而高NI的肿瘤组织中,则有更高丰度的调节性T细胞(Regulatory T cells, Tregs)、炎性巨噬细胞NLRP3 + Macro,以及肌成纤维细胞 (myofibroblastic Cancer-Associated Fibroblast, my CAF)。
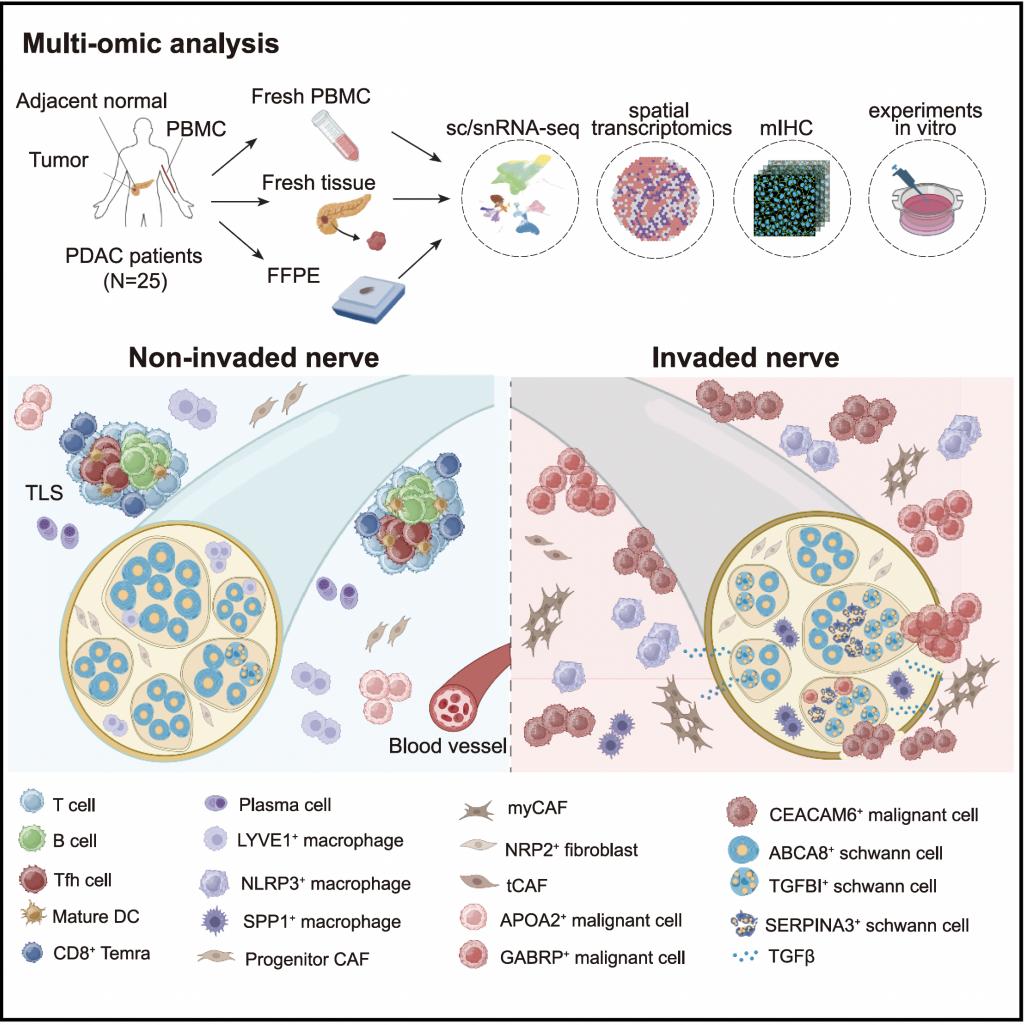
本研究首次对人肿瘤组织原位神经进行了多组学系统描绘,为日后肿瘤神经生物学的研究提供了宝贵的参考资源。其对肿瘤相关神经束内细胞组成的高分辨率刻画,鉴定出了重要的外周神经相关类群:三类施万细胞、神经内成纤维细胞、神经内组织驻留巨噬细胞、神经损伤修复巨噬细胞等。肿瘤微环境细胞对施万细胞可塑性的调控机制为理解神经-肿瘤互作提供了独特的视角。研究发现肿瘤相关神经束附近存在TLS结构,提示神经支配(Innervation)在调控抗肿瘤免疫中可能起到关键作用。这些开创性的洞察有望激发后续研究,进一步揭示神经系统、免疫组分及癌细胞在肿瘤发生、进展及转移过程中的相互作用机制。
原文链接:https://doi.org/10.1016/j.ccell.2025.06.020