近日,基础医学院病理学教研室杨雅莹/梁冰联合重庆市中医院余柯晓,在生物医学1区杂志Theranostics上发表了题为Injectable SF-platform orchestrates GPX4-targeted ferroptosis-autophagy-immunogenic circuit for overcoming oxidative resistance in triple-negative breast cancer的研究论文,报道了一种用于三阴性乳腺癌治疗的磁性可注射丝素蛋平台。该平台由磁热响应性的丝蛋白基水凝胶(IMSFs)组成,并与时序控制的TAT-Beclin1递送系统相结合。IMSFs水凝胶搭载四氧化三铁磁性纳米颗粒和索拉非尼,通过铁离子和索拉非尼的可控释放,实现局部GPX4的抑制,并通过TAT-Beclin1的局部注射促进自噬扩大铁死亡效应,最后激活免疫,有效抑制三阴性乳腺癌的增殖和转移。

研究人员通过透明质酸(HA)与丝素蛋白(SF)交联后得到可注射水凝胶(HA- SF),并将四氧化三铁磁性纳米颗粒和索拉非尼共同封装后制备得到了IMSFs水凝胶与时序控制的TAT- Beclin1协同构建磁性丝素蛋白基平台(SF-platform)。
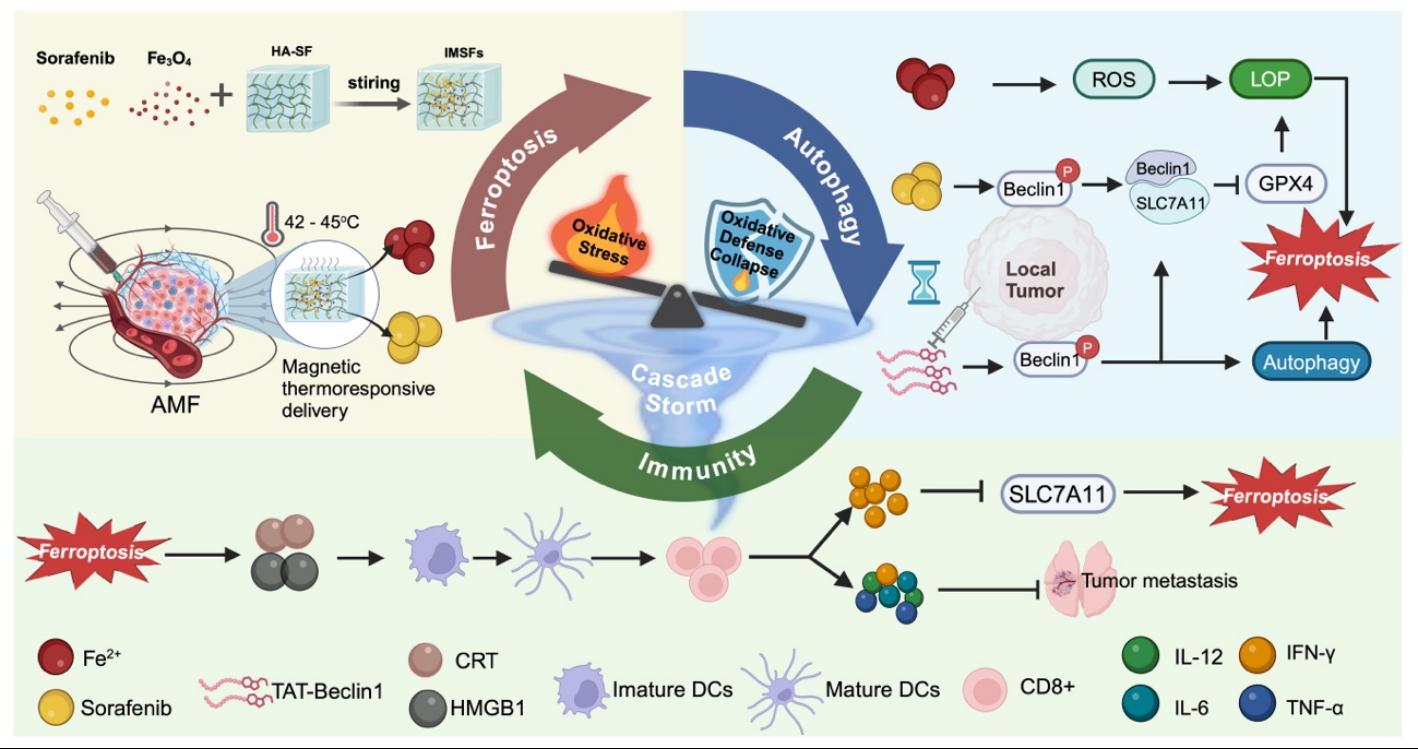
实验结果表明,该平台显示出优异的抗肿瘤疗效,并在TNBC治疗中具显示出良好的临床转化前景。首先IMSFs水凝胶在交变磁场(AMF)的作用下,可以实现肿瘤局部温和热疗并在肿瘤酸性环境下释放铁离子催化芬顿反应驱动活性氧物质(ROS)的生成。此外通过RNA测序分析发现索拉非尼的释放可以通过AMPK-Beclin1-SLC7A11轴来抑制Xc⁻系统,达到局部抑制GPX4的活性并协同促进级联性铁死亡的效应。最后研究人员通过时序控制的TAT- Beclin1局部注射的方式,在极大保留活性的同时,避免过早自噬抑制ROS的蓄积,进一步推动Beclin1-SLC7A11复合体形成放大铁死亡,通过铁死亡-自噬协同激活免疫原性细胞死亡(ICD),促进DC细胞成熟和T细胞分化,促发CD8+T细胞释放IFN-γ细胞因子下调SLC7A11表达。最终该SF- platform通过建立一个自我放大的“铁死亡-自噬-免疫”循环,推动三阴性乳腺癌氧化防御崩溃,达到抑制肿瘤生长和转移的目的。这种综合性的全新的癌症治疗模式,可以实现精准可控的靶向治疗,最大程度的提高治疗效果减少副作用。
基础医学院杨雅莹副教授、梁冰副研究员以及重庆市中医院余柯晓副主任医师为文章的共同通讯作者,基础医学院硕士研究生袁慧和附属大足区人民医院李雄武为文章的共同第一作者。该文章受到了重庆市教委青年科研项目,重庆市自然科学基金,重庆市大足区科卫联合项目的支持。
原文链接:https://www.thno.org/v15p8757.htm